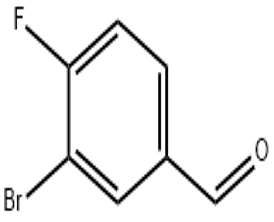
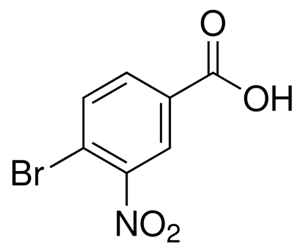
alfa-jononas (CAS Nr. 127-41-3)
| Rizikos kodai | R42/43 – Gali sukelti alergiją įkvėpus ir susilietus su oda. |
| Saugos aprašymas | S24/25 – Vengti patekimo ant odos ir į akis. |
| WGK Vokietija | 2 |
| RTECS | EN0525000 |
| TSCA | Taip |
| HS kodas | 29142300 |
alfa-jononas (CAS#127-41-3) informacija
Violetinis ketonas, taip pat žinomas kaip benzofenonas, yra organinis junginys. Štai keletas saugos informacijos apie ionone:
1. Toksiškumas: violetinis ketonas turi tam tikrą toksiškumą žmogaus organizmui. Tai gali pakenkti centrinei nervų sistemai ir kepenims, taip pat gali turėti neigiamą poveikį reprodukcinei sistemai ir embrionams.
2. Pavojus įkvėpus: įkvėpus jonono garų ar dulkių, gali atsirasti diskomforto simptomų, tokių kaip galvos svaigimas, mieguistumas, kosulys ir pasunkėjęs kvėpavimas. Ilgalaikis poveikis gali pakenkti centrinei nervų sistemai.
3. Pavojus kontaktui: Violetinis ketonas gali būti absorbuojamas per odą. Ilgalaikis arba platus sąlytis gali sudirginti odą ir akis. Dirbant su ionone reikia dėvėti tinkamas asmenines apsaugos priemones, pvz., pirštines ir apsauginius akinius.
4. Gaisro gesinimo priemonės: Nutekėjus arba gaisrui gesinti naudokite sausus miltelius, putas arba anglies dioksidą. Venkite naudoti vandens, nes violetinis ketonas reaguoja su vandeniu, sudarydamas degias dujas.
5. Atliekų šalinimas: violetinio ketono atliekas išmeskite tinkamai, laikydamiesi vietinių taisyklių ir taisyklių. Neišpilkite jo į kanalizaciją ar šiukšlių dėžę.
6. Laikymo atsargumo priemonės: Violetinį ketoną reikia laikyti vėsioje, sausoje, gerai vėdinamoje vietoje, toliau nuo ugnies šaltinių ir oksidantų.
Ši informacija skirta tik nuorodai. Jei reikia toliau naudoti arba apdoroti iononą, žiūrėkite atitinkamą saugos duomenų lapą ir pasikonsultuokite su specialistu.
gamta
Violetinis ketonas, taip pat žinomas kaip linailketonas, yra natūralus ketono junginys. Tai pagrindinis violetinių gėlių aromato komponentas.
Violetinis ketonas yra bespalvis arba šviesiai geltonas aliejinis skystis, kuris kambario temperatūroje yra lakus.
Violetinis ketonas tirpsta alkoholyje ir eterio tirpikliuose ir šiek tiek tirpsta vandenyje. Jo tankis yra palyginti mažas, jo tankis yra 0,87 g/cm³. Jis jautrus šviesai ir gali sugerti ultravioletinius spindulius.
Violetinis ketonas cheminėse reakcijose gali būti oksiduojamas į ketonų alkoholius arba rūgštis, o per hidrinimo redukcijos reakcijas gali būti redukuotas į alkoholius. Jis gali būti alkilinamas ir esterifikuojamas su daugeliu junginių.
Taikymas ir sintezės metodas
Violetinis ketonas (taip pat žinomas kaip purpurinis ketonas) yra aromatinis ketono junginys. Jis turi ypatingą kvapą ir dažnai naudojamas kvepalų ir kvepalų pramonėje. Toliau pateikiamas įvadas į jonono naudojimą ir sintezės metodus:
Paskirtis:
Kvepalai ir prieskoniai: jonono, plačiai naudojamo kvepalų ir prieskonių pramonėje violetinių kvapų gaminiams gaminti, kvapo savybės.
Sintezės metodas:
Jonono sintezė paprastai pasiekiama šiais dviem būdais:
Nukleobenzeno oksidacija: Nukleobenzenas (benzeno žiedas su metilo pakaitalu) yra veikiamas oksidacijos reakcijos, pavyzdžiui, naudojant oksiduojančią rūgštį arba rūgštinį kalio permanganato tirpalą, kad susidarytų jononas.
Pirilbenzaldehido sujungimas: Pirilbenzaldehidas (pvz., benzaldehidas su piridino žiedo pakaitais para arba meta padėtyje) šarminėmis sąlygomis reaguoja su acto rūgšties anhidridu ir kitais reagentais, kad susidarytų jononas.