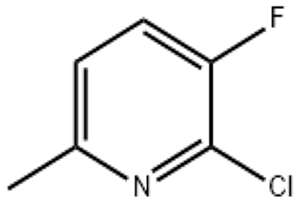
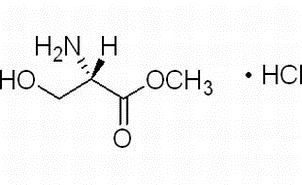
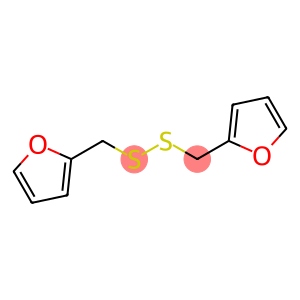
2-chlor-3-fluor-6-pikolinas (CAS Nr. 374633-32-6)
Įvadas
Išvaizda: Paprastai bespalvis arba šviesiai geltonas skystis, šios išvaizdos savybės rodo, kad jis gali būti jautrus šviesai ir šilumai, todėl būtina imtis priemonių, kad saugojimo ir transportavimo metu būtų išvengta šviesos ir temperatūros kontrolės, pvz., naudoti rudo stiklo butelius ir juos laikyti. vėsiame sandėlyje, kad būtų išvengta tolesnio spalvos pagilėjimo ir gedimo.
Tirpumas: junginys gerai tirpsta įprastuose organiniuose tirpikliuose, tokiuose kaip toluenas ir dichlormetanas, atitinka panašaus tirpumo principą ir turi afinitetą su organiniais tirpikliais dėl hidrofobinės molekulės dalies; Tačiau tirpumas vandenyje yra mažas, o stiprią vandenilio jungtį tarp vandens molekulių molekulė sunkiai veiksmingai nutraukia, todėl ją sunku išsklaidyti.
Virimo temperatūra ir tankis: Virimo temperatūros duomenys yra glaudžiai susiję su jo nepastovumu ir gali būti pagrindiniai parametrai tokioms operacijoms kaip distiliavimas ir gryninimas, tačiau, deja, konkreti virimo taško vertė nebuvo plačiai atskleista. Jo tankis yra šiek tiek didesnis nei vandens, o tankio supratimas gali padėti tiksliai įvertinti tūrio ir masės konversijos santykį atliekant eksperimentines operacijas arba pramoninius procesus, tokius kaip skysčio perkėlimas ir tikslus matavimas.
Cheminės savybės
Pakeitimo reakcija: chloro atomas ir fluoro atomas molekulėje yra potencialios reaktyvios vietos. Nukleofilinės pakaitos reakcijos metu stiprūs nukleofilai gali atakuoti vietas, kuriose yra chloro ir fluoro atomai, pakeisti atitinkamus atomus ir generuoti naujus piridino darinius. Pavyzdžiui, jis buvo derinamas su kai kuriais azoto ir sieros turinčiais nukleofilais, siekiant sukurti azoto turinčių heterociklinių junginių, turinčių sudėtingesnę struktūrą, seriją vaistų atradimui ar medžiagų sintezei.
Redokso reakcija: pats piridino žiedas yra santykinai stabilus, bet kai stiprūs oksidatoriai, tokie kaip kalio permanganatas ir vandenilio peroksidas, yra susieti su rūgštinėmis sąlygomis, gali įvykti oksidacija, dėl kurios sunaikinama arba pasikeičia piridino žiedo struktūra; Ir atvirkščiai, su tinkamu reduktoriumi, tokiu kaip metalų hidridai, teoriškai įmanoma hidrinti intramolekulines nesočiąsias jungtis.
Ketvirta, sintezės metodas
Įprastas sintezės kelias yra pradėti nuo paprastų piridino darinių ir palaipsniui sukurti tikslinę struktūrą halogeninimo ir fluorinimo reakcijose. Pradinės medžiagos piridino junginiai pirmiausia yra selektyviai metilinami ir tuo pačiu metu įvedamos metilo grupės; Tada naudokite halogeninimo reagentus, tokius kaip chloras ir skystas chloras, su tinkamais katalizatoriais ir reakcijos sąlygomis, kad būtų įvesti chloro atomai; Galiausiai, norint tiksliai fluorinti tikslinę vietą, buvo naudojami fluorinti reagentai, tokie kaip Selectfluor, kad būtų gautas 2-chlor-3-fluor-6-metilpiridinas.
Naudoja
Vaistų sintezės tarpiniai produktai: savo unikalią struktūrą pamėgo medicinos chemikai, tai aukštos kokybės tarpinis produktas kuriant naujus antibakterinius, antivirusinius ir priešnavikinius vaistus. Piridino žiedų ir jų pakaitų elektroninės savybės ir erdvinė struktūra gali specifiškai prisijungti prie tikslinių baltymų in vivo ir tikimasi, kad po vėlesnio kelių etapų modifikavimo jie bus paversti puikiai veiksmingomis veikliosiomis medžiagomis.
Medžiagų mokslas: organinių medžiagų sintezės srityje jis gali būti naudojamas gaminant funkcines polimerines medžiagas, fluorescencines medžiagas ir kt., nes gali tiksliai įvesti chloro, fluoro atomus ir piridino struktūras, aprūpinti medžiagas specialiomis elektrinėmis ir optinėmis medžiagomis. ypatybes ir skatinti pažangiausių technologijų, pvz., išmaniųjų medžiagų ir demonstravimo medžiagų, kūrimą.